Últimas Noticias
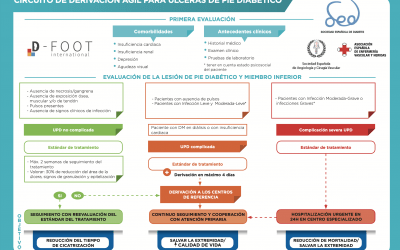
CIRCUITO DE DERIVACIÓN ÁGIL PARA ÚLCERAS DE PIE DIABÉTICO
La Asociación Española de Enfermería Vascular y Heridas avala el documento “CIRCUITO DE DERIVACIÓN ÁGIL PARA ÚLCERAS DE PIE DIABÉTICO”
Nuevo curso avalado por la AEEVH
Nuevo curso avalado por la AEEVH: Edemas y lesiones de difícil cicatrización en extremidades inferiores
Publicado un completo libro sobre la fotografía de heridas
Todo lo que necesita saber sobre fotografía de heridas en un libro gratuito
Posts recientes en nuestro blog
Estamos trabajando en nuestro nuevo Blog Científico. Próximamente publicaremos interesantes artículos para nuestra comunidad profesional.

Congresos

Formación

Guías y Documentos
Reciba nuestra newsletter en su e-mail